Código
library(Rage)
library(tidyverse)
source("R/figuras_helpers.R") # plc_save(), grviz_save(), save_plot_png()La fecundidad describe la contribución reproductiva de los individuos a la población y constituye uno de los componentes clave de los modelos de proyección poblacional. Este capítulo presenta los principios conceptuales y prácticos necesarios para calcular la fecundidad y su incorporación en matrices poblacionales estructuradas.
Por: Aucencia Emeterio-Lara y Raymond L. Tremblay
La fecundidad representa el proceso mediante el cual los individuos contribuyen nuevos reclutas a la población y es un componente esencial de la dinámica poblacional. En los modelos matriciales, la fecundidad suele integrarse como una combinación de producción reproductiva, supervivencia temprana y transición hacia los estadios iniciales del ciclo de vida.
En este capítulo se examinan los fundamentos para calcular la fecundidad a partir de datos empíricos, destacando las decisiones conceptuales necesarias para traducir observaciones biológicas, como floración, producción de semillas o reclutamiento, en parámetros demográficos coherentes. Se discuten las diferencias entre fecundidad potencial y fecundidad realizada, así como las implicaciones de estas distinciones para la interpretación de la dinámica poblacional.
Fecundidad potencial vs realizada.
Para modelos demográficos sólo es relevante la fecundidad realizada, expresada en las mismas unidades que el primer estadio del modelo.
Asimismo, se analiza cómo la fecundidad se integra en la matriz de proyección, generalmente a través de la submatriz F, y cómo su parametrización influye en el crecimiento poblacional y en análisis posteriores de sensibilidad y elasticidad. Este capítulo se diferencia de los anteriores porque se centra en la cuantificación explícita de un proceso demográfico específico, estableciendo el vínculo entre datos reproductivos y modelos poblacionales utilizados para inferir patrones de crecimiento y evaluar escenarios de manejo.
library(Rage)
library(tidyverse)
source("R/figuras_helpers.R") # plc_save(), grviz_save(), save_plot_png()Toda población de organismos depende de la reproducción para su crecimiento; sin ella, la población no puede aumentar. Por esta razón, la reproducción es un proceso esencial para evaluar el crecimiento poblacional y determinar si el reclutamiento es suficiente para sostener dicho crecimiento. En el caso de las plantas, la reproducción puede ser sexual o vegetativa. Cuando se considera el crecimiento vegetativo, es necesario incorporar una matriz de clonación. Sin embargo, en este capítulo nos enfocaremos únicamente en la reproducción sexual, que es la más común en estudios de ecología de poblaciones.
La forma en que se obtiene e integra la reproducción en los modelos de crecimiento poblacional es crucial, ya que su incorporación puede influir en los resultados y en las conclusiones derivadas del modelo. Por ello, comenzaremos describiendo errores frecuentes en el uso de matrices de transición para calcular la fecundidad. La fecundidad constituye una forma particular de transición demográfica, discutida en el capítulo sobre transiciones poblacionales. La influencia de la fecundidad sobre la dinámica poblacional se refleja directamente en la tasa de crecimiento poblacional introducida en el capítulo sobre crecimiento poblacional. La importancia relativa de la fecundidad frente a otros procesos vitales se evalúa posteriormente mediante el análisis de elasticidad poblacional.
El primer paso para calcular la fecundidad consiste en definir las clases de edad o tamaño de los individuos. Estas clases agrupan organismos con características similares en términos de edad o tamaño. Por ejemplo, en una población de peces, las clases pueden ser: juveniles, adultos jóvenes y adultos viejos; mientras que en plantas, las clases suelen ser: plántulas, juveniles y adultos. Si la primera etapa del modelo corresponde a “plántula”, el reclutamiento debe contabilizar las “nuevas plántulas” que ingresan a la población en cada periodo. Es fundamental que la etapa reproductiva se mida en la misma escala y periodo que las demás etapas.
Un error común es calcular la fecundidad usando el número de semillas producidas cuando la primera etapa del modelo son plántulas. En este caso, la fecundidad debe expresarse en términos de plántulas, no de semillas. Para ello, es necesario convertir la cantidad de semillas en plántulas mediante una tasa de germinación o de supervivencia.
La fecundidad debe expresarse en las mismas unidades que el primer estadio del modelo. Si la primera etapa es «plántula», la entrada de fecundidad cuenta nuevas plántulas por individuo reproductor, no semillas. Mezclar unidades (e.g., poner «número de semillas» en una matriz cuya primera etapa son plántulas) introduce un error sistemático que infla λ por órdenes de magnitud. Cuando sólo se conoce la producción de semillas, hay que multiplicarla por las tasas de germinación y supervivencia hasta plántula antes de incorporarla a la matriz.
A continuación se presentan los métodos y cálculos utilizados para estimar la fecundidad y su incorporación en matrices de proyección poblacional.
La fecundidad en orquídeas se refiere a la capacidad reproductiva efectiva de una población, evaluada a través de una serie de eventos: producción de flores, éxito en la polinización, formación de frutos, germinación de semillas y establecimiento de plántulas. En consecuencia, la fecundidad constituye un conjunto de procesos que determinan la viabilidad poblacional a largo plazo. Aunque puede parecer un mecanismo sencillo, en realidad es complejo, ya que depende de múltiples factores como la disponibilidad de recursos, competencia entre individuos, depredación y enfermedades.
El proceso inicia con la producción de flores, lo que implica una inversión significativa de nutrientes y agua acumulados por la planta. Además, las flores desarrollan atributos específicos para maximizar la probabilidad de polinización, tales como color, aroma, néctar y polen. Estos rasgos, sin embargo, son costosos en términos energéticos, por lo que su expresión debe ser cuidadosamente optimizada. En algunos casos, los costos reproductivos son tan elevados que pueden comprometer la supervivencia de la planta.
Diversos estudios ilustran este fenómeno. Por ejemplo, en la orquídea Comparettia falcata (Meléndez-Ackerman et al. 2000), la polinización manual mostró una correlación positiva entre el número de flores producidas y el porcentaje de frutos abortados. En Spiranthes spiralis, un año con alta producción floral se tradujo en más del 80% de individuos en estado vegetativo al año siguiente (Willems y Dorland 2000). De manera similar, en la orquídea perenne Cypripedium acaule se observó una reducción en la probabilidad de florecer y en el tamaño foliar en la temporada posterior (Primack y Stacy 1998). Otro caso se reportó en Encyclia krugii, donde el incremento en la producción de frutos se compensó en la siguiente temporada con menor crecimiento vegetativo (reducción en tamaño de hojas, número de flores, inflorescencias y mayor aborto de frutos) (Ackerman 1989).
Estos hallazgos sugieren que cada ciclo reproductivo requiere un periodo de recuperación para que la planta acumule los nutrientes necesarios para la siguiente temporada. Por lo tanto, un alto índice reproductivo —y el consecuente costo energético— puede representar una desventaja significativa, especialmente en especies con reservas limitadas.
La familia Orchidaceae exhibe una notable diversidad en sus sistemas reproductivos, incluyendo especies autógamas y alógamas (Willmer 2011, Bateman 2020). Aunque muchas orquídeas presentan barreras físicas o genéticas que limitan la autopolinización (por ejemplo, el rostelo o la incompatibilidad genética), se ha documentado que varias especies pueden utilizar su propio polen para producir frutos y semillas viables (Ackerman et al. 2023). De hecho, Catling reporta al menos 350 especies en las que alguna población se autopoliniza (Catling 1990). Se estima que aproximadamente el 31% de las especies de orquídeas producen frutos mediante autopolinización (Evans y Jacquemyn 2020), siendo esta estrategia más frecuente en especies con distribución geográfica restringida o en ambientes con escasez de polinizadores (Suetsugu 2015).
Es importante destacar que la autopolinización no implica necesariamente autogamia estricta; la mayoría de las orquídeas presentan grados variables de autogamia facultativa. Este tipo de autopolinización se ha observado bajo condiciones de estrés abiótico o disturbios antropogénicos (Talalaj y Skierczynski 2015, Tałałaj et al. 2017). Por ejemplo, las flores del género Epipactis muestran adaptaciones morfológicas que facilitan la autopolinización para asegurar la producción de semillas. Si bien la autogamia garantiza la formación de frutos, estos suelen ser más pequeños y contener menos semillas, con menor viabilidad (semillas sin embrión, embriones inviables, protocormos albinos) (Tremblay et al. 2005, Paiva Neto et al. 2022). Este fenómeno se asocia con la autocompatibilidad genética, documentada en más de 750 especies de orquídeas, incluyendo géneros como Chondrorhyncha, Coelogyne, Dendrobium, Lycaste, Notylia y Oncidium (Johnson y Edwards 2000, Tremblay et al. 2005, Barreda-Castillo et al. 2024).
Por otro lado, la polinización cruzada incrementa el éxito reproductivo al introducir diversidad genética y superar mecanismos de auto-incompatibilidad (Zhang et al. 2021). Aunque las especies autocompatibles suelen producir más frutos (Caballero-Villalobos et al. 2017), muchas orquídeas dependen exclusivamente de la polinización cruzada (Zhang et al. 2021). Por ejemplo, en la subfamilia Epidendroideae existe un alto número de especies autoestériles, mientras que en Vanilloideae y Cypripedioideae se observa producción de frutos por autopolinización, a pesar de que su morfología floral sugiere polinización cruzada (Suetsugu y Fukushima 2014, Lopes et al. 2022).
Algunas especies presentan autopolinización estricta mediante flores cleistógamas, que nunca se abren pero producen frutos fértiles, como en Lepanthes dodiana. Esta estrategia es común en plantas colonizadoras o adaptadas a ambientes extremos, donde la ausencia de polinizadores o individuos cercanos limita la polinización cruzada (Barreda-Castillo et al. 2024). La autogamia, además, requiere menos inversión energética al no producir recompensas florales (Eckert y Herlihy 2004), similar a las especies que emplean polinización por engaño, donde la ausencia de recompensas se traduce en menor éxito reproductivo (Golubov y Mandujano 2009).
Se estima que aproximadamente el 65% de las especies de Orchidaceae ofrecen algún tipo de recompensa floral (Llabrés Fernández 2015). El néctar constituye la recompensa más común para atraer polinizadores (Neiland y Wilcock 1998); sin embargo, su producción pudiese implicar un elevado costo energético para la planta, lo que puede limitar el desarrollo de otras estructuras. Ante esta restricción, muchas orquídeas han evolucionado mecanismos de polinización por engaño, estrategia presente en cerca de un tercio de las especies (entre 6,000 y 8,000) (Dafni 1983, Ackerman 1989, Tremblay et al. 2005, Case y Bradford 2009). Estas especies no ofrecen recompensa alguna, lo que reduce el gasto energético. La ausencia de recompensas permite a las orquídeas con polinización por engaño invertir recursos en otras características, como mayor número de flores, incremento en la altura de la planta y en el tamaño de la inflorescencia (Henneresse et al. 2017, Scopece et al. 2017), rasgos que aumentan la atracción visual y la frecuencia de visitas de polinizadores (Peakall 1989, Burd 1995, Aragón y Ackerman 2004, Grindeland et al. 2005, Li et al. 2011, Sletvold y Ågren 2011). Tanto la autogamia como la polinización por engaño requieren menor inversión energética al no producir recompensas (Eckert y Herlihy 2004); sin embargo, esta estrategia suele traducirse en menor éxito reproductivo. De hecho, se ha reportado que las orquídeas que emplean polinización por engaño producen, en promedio, solo la mitad de frutos en comparación con aquellas que ofrecen recompensas (Johnson y Bond 1997, Neiland y Wilcock 1998, Tremblay et al. 2005, Jersáková et al. 2006).
En los análisis de demografía poblacional, la fecundidad se ha estimado a distintos niveles: número de flores, frutos, semillas o plántulas. Algunos estudios la calculan considerando la cantidad de flores producidas por planta en relación con el número de individuos en la población, mientras que otros proponen que la producción de frutos es el indicador más preciso del éxito reproductivo (Proctor y Harder 1994).
Por ejemplo, en Dracula chimaera la fecundidad se determinó calculando la probabilidad de que una planta con flor desarrollara fruto, es decir, el número de frutos presentes en cada etapa dividido entre el total de plantas de esa misma etapa. Sin embargo, es importante subrayar que la producción de frutos no garantiza la calidad de las semillas o la presencia de semillas; por ejemplo, en la especie Psychilis krugii en Puerto Rico, la autopolinización resulta en la producción de un fruto pero las semillas están sin embrión. Además, hay muchos factores que influyen directamente en la germinación y, a largo plazo, en el establecimiento efectivo de nuevas plántulas.
El número de semillas por fruto en las orquídeas puede variar desde miles hasta millones; sin embargo, no todas son viables. Es ampliamente reconocido que una gran proporción corresponde a semillas vacías (sin embrión), mientras que otras presentan embriones no funcionales. Esto indica que no todas las semillas producidas tienen la capacidad de originar un nuevo individuo. Por esta razón, algunos estudios han incorporado la viabilidad de las semillas como un nivel adicional para estimar la fecundidad, tal como se realizó en Laelia autumnalis (Emeterio-Lara; comunicación personal).
Aunque una planta puede producir una gran cantidad de semillas viables, tras la dispersión estas enfrentan múltiples factores que limitan su éxito. Las condiciones abióticas —como temperatura, luz y humedad—, junto con factores bióticos, como las características del forófito, la disponibilidad de hongos endófitos y la presión de herbívoros o depredadores de semillas y plántulas, influyen tanto en la micorrización como en la germinación y el establecimiento de nuevas plántulas (Dressler 1993).
Estos elementos definen micrositios específicos para la germinación, que pueden incluir fisuras en la corteza de un árbol, mechones de musgo, superficies de raíces vivas o acumulaciones de humus (Rasmussen et al. 2015). A medida que las semillas atraviesan las distintas etapas de germinación, desde la imbibición hasta el desarrollo de plántulas con dos hojas (Arditti 1967), la mortalidad se mantiene en niveles muy altos. Por ejemplo, Batty et al. (Batty et al. 2001) estimaron que, en Caladenia arenicola, de aproximadamente 34,500 semillas, menos del 1% alcanzó la etapa de plántula capaz de sobrevivir a la primera sequía estival.
El reclutamiento se define como el número de plántulas que logran establecerse en el forófito y poseen el potencial de sobrevivir para avanzar a la siguiente etapa demográfica (juvenil). Las orquídeas presentan tasas de reclutamiento particularmente bajas (Larson y Batson 1978, Zotz 1998, Winkler y Hietz 2001, Garcı́a-Soriano 2003), debido a factores como la susceptibilidad al estrés hídrico durante la estación seca (Benzing 1981, Hernández-Apolinar 1992, Larson 1992, Hietz 1997, Tremblay 1997, Zotz 1998, Mondragón 2000, Garcı́a-Soriano 2003), enfermedades y depredación. Por ejemplo, en Erycina crista-galli un individuo adulto produce en promedio 0.033 plántulas/año, mientras que en Guarianthe aurantiaca un individuo reproductivo genera menos de un nuevo individuo por año.
En los modelos demográficos, alcanzar esta fase es crucial, ya que representa el valor neto de fecundidad: el número de nuevos individuos que conformarán la siguiente generación en una población natural. Sin embargo, estimar la fecundidad hasta la etapa de plántula es uno de los mayores retos, principalmente por la dificultad de asegurar la identidad de la especie. Un aspecto clave es la proximidad a la planta madre, dado que, aunque el viento favorece la dispersión a larga distancia, la mayoría de las semillas se depositan cerca de ella (Chung et al. 2004, Trapnell et al. 2004, Jersáková y Malinová 2007).
A pesar de estas limitaciones, existen estudios que han registrado plántulas sobrevivientes tras un periodo (generalmente un año). Ejemplos incluyen Brassavola cucullata (Ackerman et al. 2020) y E. crista-galli (Maldonado Flores 2006), donde la fecundidad se estimó dividiendo el número de nuevos reclutas observados en campo entre el número máximo de frutos reportados durante el periodo de estudio. En otros casos, como Guarianthe aurantiaca, se calculó comparando los reclutamientos entre años consecutivos (Mondragón 2009). Estos datos proporcionan estimaciones más precisas para proyectar la dinámica poblacional y diseñar estrategias de conservación.
Una flor no es un fruto, un fruto no es una semilla viable, una semilla no es una plántula. La fecundidad efectiva en orquídeas resulta de una cadena de filtros sucesivos: producción floral → polinización exitosa → cuajado de fruto → producción de semillas con embrión → germinación → establecimiento. En cada paso, la mortalidad puede ser muy alta (p. ej., en Caladenia arenicola menos del 1% de las semillas llega a plántula). Asumir que un fruto observado equivale a una plántula establecida sobreestima la fecundidad realizada en varios órdenes de magnitud.
Tabla de algunos ejemplos de fecundidad en orquídeas, donde se muestra la especie, el índice de fecundidad y la referencia del estudio.
| Especie | Indice de Fecundidad | Referencia |
|---|---|---|
| Lepanthes eltoroensis | Cantidad de Plántulas / Adultos reproductivos | Tremblay y Hutchings (2003) |
| Erycina crista-galli | 0.033 plántulas/año | Maldonado Flores (2005) |
| Encyclia tampensis | 0.1 plántulas/fruto | Larson (1992) |
| Guarianthe aurantiaca | <1 plántula/año | Mondragón (2009) |
Los estudios disponibles indican que las orquídeas presentan un crecimiento lento, requiriendo entre 8 y 19 años para alcanzar la madurez reproductiva (Hernández-Apolinar 1992, Larson 1992, Zotz 1995, 1998). Sin embargo, existen excepciones, como las orquídeas miniatura o de ramilla (principalmente Pleurothalliinae), que pueden madurar en uno o pocos años (1-3 años) (Chase 1987), en contraste con los 8-19 años requeridos por las especies de mayor tamaño.
Para estimar el crecimiento y la edad reproductiva en Lycaste aromatica, se ha utilizado la producción regular de pseudobulbos, los cuales permanecen varios años en la planta. Con base en este patrón, se predice que Encyclia tampensis alcanza la floración aproximadamente a los 15 años. No obstante, bajo condiciones controladas de cultivo, la fase de pre-bulbo puede durar entre 0.5 y 2 años, y la primera floración ocurrir en tan solo 5 a 6 años (H. Lutero, comunicación personal).
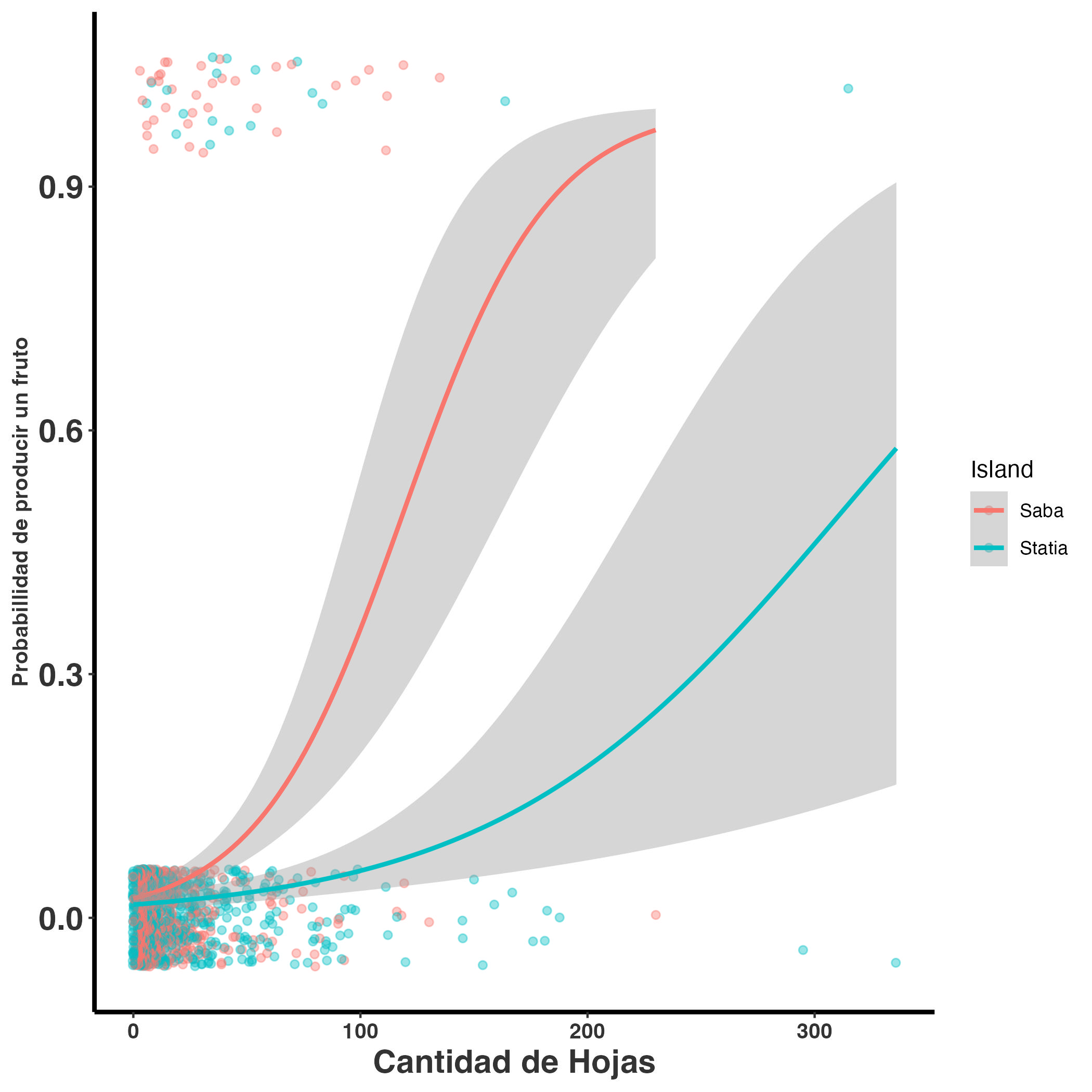
Un caso interesante se observa en Brassavola cucullata, una especie rupícola y epífita de las Antillas Menores. En esta orquídea, los pseudobulbos presentan hojas lanceoladas, y la probabilidad de floración no depende de la longitud de las hojas, sino de la cantidad de hojas por individuo. De hecho, el número estimado de hojas constituye un buen predictor de la capacidad de una planta para producir flores, aunque se han registrado diferencias en esta relación entre las poblaciones de las islas Saba y San Eustaquio.
En este ejemplo, la primera fila de la matriz representa la fecundidad de la población en la posición (3,1) (columna, fila), correspondiente al número promedio de semillas producidas por un individuo adulto. Sin embargo, la fecundidad en modelos demográficos debe expresarse en términos de plántulas, no de semillas. Por ello, es necesario convertir la cantidad de semillas producidas en plántulas mediante una tasa de germinación o una tasa de supervivencia hasta la etapa de plántula. De lo contrario, el cálculo presentará un sesgo, ya que se estaría estimando fecundidad con base en semillas, sin considerar su capacidad real de generar nuevos individuos.
matA_sem <- rbind(
c(0.0, 0.0, 1000), # fecundidad 1000 semillas en promedio por adulto
c(0.5, 0.0, 0.0),
c(0.0, 0.4, 0.0)
)Visualizamos el ciclo de vida de la población con la función plot_life_cycle() de la librería Rage:
etapas <- c("plántula", "juvenil", "adulto")
plc_save(matA_sem, stages = etapas, fontsize = 5, png = "images/fec-life-cycle-1.png")matA_sem con los estadios plántula, juvenil y adulto.
Una alternativa para estimar la fecundidad en términos demográficos consiste en calcular el número de nuevas plántulas que se incorporarán en el siguiente periodo, utilizando una tasa de germinación y una tasa de supervivencia hasta la etapa de plántula.
Por ejemplo, si:
entonces la fecundidad en términos de plántulas se calcula como:
\[\text{Fecundidad} = \frac{(1000 \times 0.5 \times 0.2)}{75} = 1.33\]
Esto significa que, en promedio, cada adulto contribuiría con 1.33 plántulas al siguiente periodo.
Por consecuencia la matriz cambia a:
matA_pl <- rbind(
c(0.0, 0.0, 1.333),
c(0.5, 0.0, 0.0),
c(0.0, 0.4, 0.0)
)
etapas <- c("plántula", "juvenil", "adulto")
plc_save(matA_pl, stages = etapas, fontsize = 5, png = "images/fec-matA-pl.png")matA_pl con fecundidad de 1.333 plántulas por adulto.
Otra alternativa consiste en calcular la fecundidad directamente en función del reclutamiento observado, utilizando el número de plántulas establecidas en el periodo siguiente. Este método es útil cuando no se dispone de información sobre la producción de semillas ni sobre sus tasas de germinación y supervivencia.
La estimación se obtiene dividiendo el número total de plántulas registradas en el periodo \(t_2\) entre el número de adultos presentes en el periodo anterior \(t_1\). Por ejemplo, si en \(t_2\) se contabilizan 50 nuevas plántulas y en \(t_1\) había 100 adultos, la fecundidad sería:
\[\text{Fecundidad} = \frac{50}{100} = 0.5\]
Esto indica que, en promedio, cada adulto contribuyó con 0.5 plántulas a la siguiente generación.
matA_pl2 <- rbind(
c(0.0, 0.0, 0.5), # fecundidad 0.5 plántulas en promedio por adulto
c(0.5, 0.0, 0.0),
c(0.0, 0.4, 0.0)
)
etapas <- c("plántula", "juvenil", "adulto")
plc_save(matA_pl2, stages = etapas, fontsize = 5, png = "images/fec-matA-pl2.png")matA_pl2 con fecundidad de 0.5 plántulas por adulto.
Tres maneras de estimar la fecundidad, ordenadas de la más exigente a la más práctica.
La vía directa absorbe automáticamente las pérdidas a lo largo de la cadena reproductiva, pero asume que las nuevas plántulas provienen de los adultos del periodo anterior y no de inmigración o banco de semillas.
Para estimar la fecundidad en modelos poblacionales, es necesario asumir ciertos supuestos fundamentales.
Cuatro supuestos que se asumen al estimar fecundidad por reclutamiento directo.
Si alguno de estos supuestos se rompe, la fecundidad estimada será sesgada. Conviene evaluar la plausibilidad de cada uno para la especie y el sitio antes de aceptar el valor obtenido.
Es importante reconocer que no existe un método perfecto para calcular la fecundidad. El procedimiento descrito aquí es útil cuando no se dispone de información sobre la cantidad de semillas producidas ni sobre su supervivencia y germinación. Sin embargo, siempre existe la posibilidad de que algunas semillas germinen en otros periodos o provengan de sitios externos, lo que introduce sesgos. Mientras estos sesgos sean mínimos, las estimaciones pueden considerarse aceptables para expresar la fecundidad en términos de plántulas.
El escenario ideal sería seguir todo el proceso reproductivo: cuantificar el esfuerzo reproductivo de cada individuo, registrar la producción de semillas y monitorear su germinación en campo. No obstante, este seguimiento completo es prácticamente imposible, por lo que se deben asumir ciertos procesos biológicos, entre ellos: